De acuerdo con los últimos datos de la Organización Mundial de la Salud, se conocen más de ochenta enfermedades autoinmunes y se sabe que afectan entre el 3 y el 7 por ciento de la población occidental.
Dentro de esta gran cantidad, estos
trastornos afectan desproporcionadamente a las mujeres, que representan casi el
80 por ciento de los casos. A menudo las afectan en edad fértil por lo que se
convierten en una complicación para el embarazo. Las razones de este panorama
desigual todavía no son comprendidas por los médicos en profundidad.
El sistema inmune es una compleja red de células y componentes celulares, llamados moléculas, que normalmente trabajan para defender al organismo y eliminar infecciones causadas por bacterias, virus y otros microorganismos invasores.
La palabra “auto” proviene del griego y quiere decir uno mismo. En una persona con una enfermedad autoinmune, su sistema inmunitario ataca erróneamente a células, tejidos y órganos de su propio organismo.
Se produce cuando el sistema inmune funciona
incorrectamente y el organismo no distingue entre lo propio del cuerpo y lo
ajeno, entonces altera su funcionamiento correcto y puede poner en riesgo la
vida.
El sistema inmune produce un tipo de célula
que secreta auto-anticuerpos que pueden unirse a las células y tejidos del
cuerpo. En las personas con un sistema inmunitario sano, varios mecanismos
mantienen estas células en jaque y las expulsan del cuerpo. Sin embargo, el
proceso puede no funcionar correctamente. Cuando esto sucede, estas células
proliferan, produciendo auto-anticuerpos de más, y se produce una enfermedad
autoinmune como resultado.
Estos auto-anticuerpos pueden dañar las
articulaciones, el sistema digestivo, el corazón, los pulmones, los riñones,
los nervios, folículos pilosos, el tejido conectivo en la piel y los vasos
sanguíneos. Aunque cada trastorno es distinto, comparten con frecuencia
síntomas tales como la fatiga, los mareos y fiebre baja. La inflamación es una
característica de todos ellos, tanto en el sitio donde se produce la
enfermedad, como en las articulaciones y en la sangre.
Entre las enfermedades autoinmunes más
comunes están la artritis reumatoidea,
que ataca el revestimiento de las articulaciones, la diabetes tipo 1, que destruye las células necesarias para
controlar el azúcar en la sangre y la esclerosis
múltiple, que daña revestimientos alrededor de los nervios. También se
presentan la enfermedad de Crohn,
que ataca el tracto gastrointestinal, la esclerodermia, que provoca el crecimiento anormal de tejido
conectivo en la piel y vasos sanguíneos, la psoriasis, en el que las nuevas células de la piel se dañan, la enfermedad de Hashimoto, que afecta a
la glándula tiroides y el lupus
eritematoso sistémico, que puede dañar las articulaciones, la piel, el corazón,
los pulmones y los riñones.
Las enfermedades
autoinmunes siguen siendo un misterio para la ciencia. Hasta el momento se conocen sus
síntomas y su desarrollo, pero se ignora lo que las produce y la mayoría de
ellas se puede tratar, pero no curar. Hay hipótesis al respecto, pero ninguna
de ellas está totalmente comprobada. Lo que sí se sabe es que la mente desempeña un
papel importante en estas patologías.
Lo que resulta
desconcertante en las enfermedades autoinmunes es que son el resultado de un
ataque del cuerpo sobre sí mismo. El organismo se comporta como si los antígenos propios fueran virus
invasores y los ataca. En otras palabras, falla el sistema de reconocimiento de
lo propio y de lo ajeno. Esto ocurre en personas que están perfectamente sanas
y la medicina todavía no sabe por qué.
La interacción entre la genética y las
experiencias de la vida temprana moldean, literalmente, los circuitos del
cerebro en desarrollo el cual es contundentemente influenciado por la
sintonización o falta de ella, entre el adulto y el niño, sobre todo en los
primeros años de vida. Los ajustes fisiológicos y psicológicos de corto plazo a
los que recurrimos para sobrevivir en esta primera etapa tienen consecuencias
de largo plazo sobre el aprendizaje, el comportamiento, la salud y la
longevidad.
Las interacciones entre cerebro y cuerpo
también determinan que las circunstancias y experiencias adversas durante la
infancia temprana – incluso en útero – dejan no solo efectos psicológicos de
largo plazo, sino que también pueden ser promotoras de enfermedad. Numerosos
estudios demuestran que el sufrimiento de los primeros años de vida potencia
muchísimas enfermedades, desde mentales, como depresión, psicosis o adicciones,
hasta trastornos autoinmunes y cáncer.
Las enfermedades autoinmunes afectan más a
las mujeres
Las mujeres suelen tener una respuesta inmune
más fuerte que los hombres a las infecciones y vacunas, ya que producen niveles
más altos de anticuerpos. En el caso de los trastornos autoinmunes, ese rasgo
parece ser contraproducente. "La inmunidad robusta en las mujeres puede
ser buena evolutivamente, pero el exceso de inmunidad puede ser malo si se
dirige hacia sí mismas", explicó Rhonda Voskuhl, profesora de neurología
de la Universidad de California en Los Ángeles, que estudia la esclerosis
múltiple.
Los científicos creen también que las
hormonas sexuales pueden desempeñar un papel importante, debido a que muchos
trastornos autoinmunes se producen en mujeres poco después de la pubertad.
Algunos estudios, de hecho, indican que las hormonas femeninas – estrógeno y
prolactina – estimulan el crecimiento de células que producen anticuerpos. Por
otro lado, la comunidad científica también estima que los cromosomas sexuales,
específicamente el cromosoma X, pueden influir en la propensión.
Los síntomas de algunas enfermedades
autoinmunes, como el lupus, a menudo empeoran durante el embarazo, mientras que
en otros, como la artritis reumatoidea, pueden mejorar. No es raro que las
mujeres tengan su primer episodio de lupus durante el embarazo. Probablemente
se habría desarrollado de todos modos, pero tiende a surgir durante el embarazo.
La relación entre las enfermedades
autoinmunes y la menopausia es aún más estrecha. Hay una cierta incidencia de
mujeres que contraen una enfermedad autoinmune después de la menopausia, lo que
indica que el problema no son las hormonas.
Las enfermedades autoinmunes y los mecanismos
psicosomáticos
La ciencia señala
que las enfermedades autoinmunes son el resultado de múltiples factores, dentro de los cuales la genética desempeña
un papel importante. Sin embargo, hasta el momento no hay evidencias
contundentes de que esto sea así. En cambio, sí se ha probado que la mente
tiene un papel decisivo en tales patologías, especialmente en cómo la
experiencia subjetiva es la que produce la enfermedad.
Actualmente las enfermedades autoinmunes son abordadas por la mayoría de los
profesionales como enfermedades psicosomáticas. Esto quiere decir que se
trata de males que tienen su origen en la mente y que toman forma a través del
cuerpo.
Hay diferentes enfoques al respecto. Algunos
sostienen que se trata de una incapacidad esencial para verbalizar las
emociones. Otros indican que es una respuesta defensiva contra la
desintegración emocional. También se aborda como un “delirio corporal”, cuyo
antecedente es la depresión, o como una respuesta a un conflicto insoluble.
Sea cual sea el enfoque, lo cierto es que el
punto en común es la comprobación de que hay realidades que existen en la mente de las personas y que encuentran
una vía de manifestación a través de la enfermedad en el cuerpo.
Las enfermedades
autoinmunes son insidiosas y dañan notablemente calidad a la vida. Suelen ser dolorosas, de
difícil asimilación y poco esperanzadoras. Lo peor es que quienes las sufren
acuden al médico en busca de respuestas y, por lo general, solo encuentran
silencios y paliativos, no siempre eficaces, para sus padecimientos. Sin
embargo, cada vez resulta más claro que la salud y el bienestar son conceptos
integrales, en los que tiene tanta importancia el plano físico como el plano
mental.
La salida para una
persona con una enfermedad autoinmune es precisamente dejar de creer que es una
pastilla, una vitamina o algún médico milagroso lo que logrará restaurar su
salud. No es que no
deba acudir a estas soluciones, sino que en su tratamiento de base debe existir
la intervención de un profesional de la salud mental.
Todas las enfermedades tienen un componente
emocional y mental involucrado, pero en las autoinmunes este factor es
absolutamente decisivo. La resistencia
a tratar su enfermedad como un tema de la psiquis es, seguramente, la razón
fundamental por la que no encuentran alivio para sus sufrimientos
físicos.
Una resistencia que nace de la idea
equivocada de que aquel que sufre una enfermedad con una base mental es porque
no es lo suficientemente fuerte y se apoya en una idea aún más equivocada: este
dolor es una invención del paciente.
La influencia de las emociones en las
enfermedades autoinmunes
Las enfermedades
autoinmunes ponen en marcha un mecanismo de autodestrucción. Es el propio cuerpo el que deja
de reconocer los antígenos que le pertenecen y comienza a auto-atacarse, como
si lo que lleva dentro de sí fuera amenazante o peligroso.
La mente es tan importante en estos procesos,
que incluso ha surgido una nueva disciplina para tratar estos males, la cual se
conoce con el nombre de psiconeuroinmunología. Así, lo cierto es que las enfermedades autoinmunes no solamente
suelen ser crónicas, sino que también resultan incapacitantes y
pueden llevar a una persona hasta la muerte.
Los estudios realizados sugieren que quienes
padecen este tipo de enfermedades generalmente tienen un alto nivel de
depresión, pero ésta no siempre es evidente. Dicho de otro modo, puede que se
trate incluso de alguien risueño y vital, pero en el fondo lleva una gran
insatisfacción que, generalmente, ni él mismo reconoce.
Otro de los rasgos
frecuentes es cierta incapacidad para reconocer las propias emociones. Bien sea por una excesiva
intelectualización o racionalización de las situaciones o bien porque se trata
de personas que quieren tener todo bajo control y experimentan los afectos como
amenazas a su autonomía.
La psiconeuroinmunología
Es una rama de la ciencia que estudia las
complejas inter-relaciones entre el sistema nervioso central – que controla procesos
biológicos y psíquicos – y el sistema inmune. Se fundamenta en el estudio de
los mecanismos de interacción entre el cerebro y el cuerpo, es decir entre los
diferentes sistemas fisiológicos responsables de la homeostásis: el sistema
nervioso, el sistema inmune y el sistema endocrino.
En las paredes del intestino delgado existen
amplias redes neuronales, el Sistema
Nervioso Entérico. Este sistema entérico no sólo está formado por
neuronas que tapizan la mucosa intestinal, sino principalmente por células
gliales. Estas neuronas también son capaces de sintetizar hormonas,
neurotransmisores y otras sustancias químicas.
En condiciones normales, a excepción de las
benzodiacepinas endógenas – endorfinas y encefalinas –, no existe ninguna
constatación científica de que estos neurotransmisores atraviesen la barrera
hematoencefálica, por lo que no deberían ocasionar ningún efecto a nivel del
Sistema Nervioso Central. Sin embargo, cambios en la permeabilidad de la
barrera hematoencefálica, como en casos de estrés crónico, patologías
inflamatorias cerebrales o sistémicas que producen un aumento de citoquinas, o
alguna forma de transporte o mecanismo físico-químico de momento no encontrado,
permitiría atravesarla y por lo tanto influenciar en las funciones del Sistema
Nervioso Central.
Independientemente de las probables
comunicaciones establecidas a través de los neurotransmisores sintetizados en
el intestino, las informaciones sensitivas del sistema digestivo llegan a
núcleos neurovegetativos del tronco cerebral, de aquí al tálamo – centro
integrador de todas las informaciones sensitivas – y finalmente al córtex
sensitivo. El tálamo a su vez está interconectado con estructuras del sistema límbico – origen de las respuestas emocionales – y también con el hipotálamo – sede de
los instintos primarios de supervivencia regulados a través del sistema neurovegetativo
y neurohormonal (neuroejes hipotálamo-hipofisarios) –. Estos centros superiores
ejercen una inhibición descente o facilitan la modulación de las
funciones y reflejos digestivos (vómito, defecación…).
El Sistema Nervioso Central y el propio
Sistema Nervioso Entérico pueden producir una sensibilización del Sistema Nervioso Entérico, ocasionando
desequilibrios en los niveles de los neurotransmisores, lo cual facilita la
aparición de disfunciones gastrointestinales, patologías inflamatorias
intestinales, intolerancias alimentarias, enfermedades autoinmunes. Los
leucocitos tienen receptores para casi todos los neurotransmisores,
especialmente para la serotonina y la dopamina.
*
*
Científicos descubren un nuevo vínculo entre
el cerebro y el sistema inmunológico
Un equipo de investigadores de la Escuela de
Medicina de la Universidad de Virginia (UVA), en un estudio publicado en la
revista Nature de junio 2015, han hecho un descubrimiento que, según
ellos, podría cambiar los libros de texto: Han determinado que el cerebro está
conectado directamente al sistema inmunológico por vasos linfáticos cuya
existencia, hasta ahora, no se conocía.
El hecho de que estos vasos no hayan sido
detectados hasta la fecha, a pesar de que el sistema linfático – que contribuye
de manera principal a formar y activar el sistema inmunitario – ha sido mapeado
a fondo en todo el cuerpo, resulta sorprendente ya de por sí, pero la verdadera
importancia del hallazgo radica en los efectos que podría tener para el estudio
y el tratamiento de enfermedades neurológicas como el autismo, la
enfermedad de Alzheimer o la esclerosis múltiple.
El cerebro es como cualquier otro tejido
conectado al sistema inmune, en este caso a través de los vasos linfáticos
meníngeos. Las meninges son las membranas que recubren el cerebro. Se cree que,
para cada enfermedad neurológica con un componente inmune, estos vasos pueden desempeñar
un papel importante.
El descubrimiento ha sido posible gracias a
la labor de Antoine Louveau, becario post-doctoral del laboratorio Kipnis quien inventó
un método ingenioso para la visualización de las meninges del cerebro de un
ratón sin destruirlo. Esto permitió detectar los vasos a través de un
microscopio. Se describen los vasos
linfáticos en los tejidos del cadáver de un ratón. Los vasos
linfáticos se complementan con los vasos sanguíneos del cuerpo, llevando las
células inmunes por todo el cuerpo a través de la sangre.
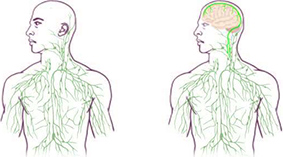 |
Mapa del sistema linfático: viejo (izquierda) y
actualizado (derecha) para reflejar el descubrimiento
|
Estos vasos linfáticos cerebrales han podido
permanecer ocultos todo este tiempo porque estaban bien escondidos, ya que
siguen a un vaso sanguíneo principal hacia los senos, un área que es difícil de
registrar en imágenes.
El microbioma intestinal está separado del
torrente sanguíneo por el revestimiento de los intestinos, y desde el cerebro
por la barrera hematoencefálica. Pero en los últimos veinte años, la idea de
que el cerebro está inmunemente privilegiado, ha sido desmantelada poco a poco. Estudios
han demostrado que el cerebro interactúa con el sistema inmune periférico, aunque sea en formas únicas. Las
células inmunes, de alguna manera, circulan a través del cerebro, y los
antígenos que normalmente serían producidos por una respuesta inmune, van
desde el cerebro a los ganglios linfáticos.
La presencia inesperada de estos vasos
linfáticos plantea un enorme número de preguntas que ahora necesitan
respuestas, tanto sobre el funcionamiento del cerebro como sobre las
enfermedades que afectan a dicho funcionamiento. Por ejemplo, en el caso de la
enfermedad de Alzheimer hay acumulaciones de grandes porciones de proteínas en
el cerebro. Creen que estas se pueden acumular porque no están siendo
eliminadas eficazmente por los vasos encontrados.
Estos conductos además varían con la edad,
por lo que el papel que desempeñan en el envejecimiento es otra vía por
explorar. Además, otras enfermedades neurológicas, desde el autismo a la
esclerosis múltiple, deberían ser reconsideradas ahora, a la luz de la
presencia de algo que la ciencia insistió en que no existía.
Las enfermedades autoinmunes aumentan con el
estrés crónico
Investigadores de la universidad Ben Gurion, en
un estudio publicado en el European
Journal of Immunology de marzo 2014, han demostrado la relación entre el
estrés crónico y las enfermedades causadas por el sistema inmunitario.
La investigación ha sido realizada en ratones
a los que se ha sometido a situaciones
de fuerte estrés. Ante esta situación, los ratones liberaban unos niveles
más elevados de gluco-corticoides de lo normal, lo que provocaba un mal funcionamiento de su sistema inmune.
El estudio también pudo revelar que este proceso se da con más frecuencia en
mujeres que en hombres, algo que explicaría, según los científicos, la gran
cantidad de féminas con enfermedades autoinmunes.
El estrés crónico, junto a otros factores
como la genética y el entorno, pueden dañar el funcionamiento del sistema
inmunológico, que es importante pues regula su defensa e impide que sea atacado.
Este mecanismo parte del cerebro, del hipotálamo. Los corticoides se suelen
usar en el tratamiento de las enfermedades autoinmunes pero este estudio ha
demostrado que en situaciones de estrés no solo no ayudan a curarlas sino que
las potencian.
Un estudio descubre nuevas conexiones entre
la microbiota intestinal y las enfermedades autoinmunes
Una investigación del CSIC (Consejo Superior
de Investigaciones Científicas) de España, en un estudio publicado en la revista mBIO de
octubre 2014, ha descifrado el perfil de la microbiota intestinal en
pacientes de LES (lupus eritematoso sistémico).
El lupus eritematoso sistémico (LES) es una
enfermedad autoinmune crónica que provoca que el sistema inmunológico ataque
erróneamente al tejido sano del cuerpo. Puede afectar la piel, las
articulaciones, los riñones, el cerebro u otros órganos.
Los resultados muestran un desequilibrio en
la ratio de los dos grupos de microorganismos más abundantes en el intestino
humano – los Bacteroidetes y los Firmicutes –, a favor del
primero, mientras que la carga y diversidad bacteriana eran similares entre los
pacientes y el grupo de control.
Para este estudio se comparó un grupo de 20
pacientes con LES de una zona geográfica concreta (Asturias) con otro similar
de personas sanas, teniendo en cuenta factores como la edad, el sexo, la
medicación y su historial médico. El grupo con LES incluía individuos con una
amplia variedad de síntomas, lo cual permitió establecer una serie de
correlaciones entre el perfil microbiano y la patología.
Existen cada vez más pruebas de que la
microbiota podría tener un impacto sobre los síntomas y la progresión de algunas
enfermedades autoinmunes, afirman los investigadores en sus conclusiones. Sin
embargo sigue sin aclararse el cómo y el porqué de la influencia de esta comunidad
microbiana sobre el LES.
Se sabe, por ejemplo, que el perfil
microbiano intestinal podría modularse a través de patrones alimentarios como
intervenciones dietéticas para favorecer el incremento de las poblaciones
microbianas que tengan incidencia en la sintomatología del LES.
Hallan cómo frenar la intensidad de la
respuesta inmune para tratar las enfermedades autoinmunes
Un estudio llevado a cabo por investigadores
del Instituto Salk de Estudios Biológicos en La Jolla (EE.UU.), publicado en la
revista Neuron de enero 2017, muestra
que para frenar la destrucción del sistema inmune habría que inhibir una
enzima denominada ‘escramblasa 1 de los fosfolípidos’ (PLSCR1).
Por
lo general, el sistema inmune reconoce y actúa rápidamente frente a una amenaza
potencial como son las células infectadas por un virus. Sin embargo, y
actuando sobre la PLSCR1, los investigadores han sido capaces de proteger a las
células infectadas del ataque inmunitario y de incrementar la expresión de un
virus diseñado por ingeniería genética por un periodo de hasta seis meses,
creando así el potencial para terapias mucho más duraderas.
 |
| Fago – virus sanadores |
Tras millones de años de evolución, los virus
se han especializado en entrar en las células y utilizar su maquinaria
molecular para su propio beneficio. Un aspecto que están aprovechando en los
últimos años los científicos para manipular estos virus y emplearlos como
vectores para transportar material a las células, ya sea un gen – que se
insertará en el ADN celular – o un fármaco. Pero terapéuticos o no, no dejan de
ser virus, por lo que también serán rastreados y atacados por el sistema
inmune.
Para evitar que las células inmunes no ataquen
estos virus ‘sanadores’ y puedan llevar a cabo su beneficio, los autores han
centrado su investigación en la respuesta inmune en el cerebro. Y para ello,
inyectaron un adenovirus manipulado genéticamente en el cerebro de un modelo
animal – ratones – para observar las
señales emitidas tanto por las células infectadas como por las células inmunes
y analizar las proteínas producidas en respuesta a la infección.
Una vez es infectada, la célula emite señales
de socorro, en caso de la exposición en su membrana externa de un lípido denominado
‘fosfatidilserina’ que atrae a las células inmunes del cerebro – las microglías –. Las microglías evalúan si aislar a la célula infectada – lo que supone un
riesgo de expansión de la infección a las células circundantes – o destruirla – lo que puede suponer un problema dado que la función de esta célula cerebral
puede ser muy importante y, una vez eliminada, no se regenera –.
Así, y con objeto de conocer los pormenores
de esta decisión de las microglías, los autores alteraron los niveles de las
proteínas implicadas en la comunicación – o ‘señalización’ – tanto intra como
extracelular.
Los resultados mostraron que la reducción de
los niveles de PLSCR1 provocó una gran variedad de cambios en la respuesta
inmune: las microglías se mantuvieron a
una distancia prudente, pero sin intervenir, y se disminuyó la producción de
citoquinas – proteínas que promueven la inflamación – sobre todo al
convocar a más células inmunes al combate.
La PLSCR1 actúa transportando la
fosfatidilserina al exterior de la membrana celular, activando la señal de
socorro.
Las infecciones. Los resultados también mostraron
que los efectos protectores de la inhibición de PLSCR1 se mantuvieron durante
seis meses, el periodo máximo alcanzado hasta el momento con cualquier
manipulación de las proteínas implicadas en la respuesta inmune. Un aspecto que
resulta muy importante dado que PLSCR1 no es exclusiva del cerebro, sino que se
encuentra en todo el organismo. Tal es así que los autores creen que, más allá
de facilitar el transporte de tratamientos a través de los virus, los
resultados podrían aplicarse a otros trastornos inflamatorios – como las infecciones – e, incluso, a las
enfermedades autoinmunes y las patologías neurodegenerativas – caso del
Alzhéimer –.
Solo hay que
imaginar la posibilidad de desarrollar un fármaco inhibidor que un paciente
podría tomar para frenar el exceso de inflamación, lo que tendría un efecto
beneficioso enorme sobre un gran número de enfermedades.
*
*
Influencia de la dieta y la nutrición en las
enfermedades autoinmunes
Los problemas autoinmunes tienen una fuerte
predisposición genética pero los desencadenantes pueden ser sol excesivo,
infecciones, drogas u otras condiciones – como el embarazo – que estresan el
cuerpo.
La
evidencia creciente indica un papel de la dieta en la prevención, retraso o
inversión de enfermedades autoinmunes determinadas genéticamente.
Como el intestino es un sitio importante de
muchas interacciones complejas que controlan la inmunidad, es el mayor interfaz
entre un individuo y su medio ambiente, y, por lo tanto, ofrece la mayor
exposición para la construcción de micro-organismos inmunes y la exposición a
toxinas y alérgenos. Somos lo que comemos. Esto sugiere un papel importante de
los probióticos y prebióticos en la autoinmunidad.
Las dietas maternas durante el embarazo y la
lactancia también influyen en los procesos autoinmunes. La lactancia materna
emerge como un factor potencialmente protector para la prevención de alergias y
la enfermedad celíaca.
En los últimos años, la evidencia ha
demostrado un papel importante de factores específicos de la dieta, como la
vitamina D, la vitamina A, selenio, zinc, ácidos grasos omega-2, probióticos,
glutamina (un aminoácido) y los flavonoides (sustancias químicas de plantas que
protegen contra la enfermedad) en las enfermedades autoinmunes. La deficiencia
de vitamina D se ha asociado con aumento de la autoinmunidad y mayor
susceptibilidad a las infecciones. Asociaciones entre la vitamina D y
enfermedades autoinmunes han sido confirmadas en esclerosis múltiple y artritis
reumatoide.
Estudios recientes también indican que la
vitamina A es un potente inmuno-regulador y puede ser instrumental en la
prevención de la inflamación intestinal y la autoinmunidad. La modificación de
la dieta ha demostrado su mayor efecto beneficioso cuando se inicia antes o
inmediatamente después de la aparición de la enfermedad. Óptima pero
equilibrada la ingesta de alimentos mantiene un crecimiento saludable y la vida
libre de enfermedad.
Deficiencias de nutrientes relacionadas con
enfermedades autoinmunes
Si sufrimos de deficiencias de nutrientes clave, corremos el riesgo de que
nuestro sistema inmune se desboque y ataque los propios tejidos del cuerpo y
lleve a la autoinmunidad.
Vitamina D. Regula y previene la autoinmunidad al
estimular las células T reguladoras, que son responsables de diferenciar entre
invasores peligrosos y células “propias”. Cuando la vitamina D promueve estas
células, le enseña al sistema inmune a no atacarse a sí mismo. La
vitamina D también es compatible con la capacidad para combatir las infecciones
virales y bacterianas que pueden desencadenar o empeorar las condiciones
autoinmunes.
Omega 3. Los estudios han demostrado que los aceites
omegas 3 mejoran la activación de las células B y seleccionan la producción de
anticuerpos, lo que puede reducir la respuesta inflamatoria y ayudar al sistema
inmunológico a combatir los patógenos.
Vitaminas B. Las vitaminas B no solo proporcionan energía
a nuestras células. También controlan la función inmune, las hormonas, el
estado de ánimo, el sueño, los nervios, la circulación y la digestión. La vitamina
B12, por ejemplo, es compatible con la producción de glóbulos blancos, que son
componentes esenciales del sistema inmune.
Selenio. El selenio puede ser un mineral poco
conocido, pero los estudios demuestran que es esencial para regular la respuesta
inmune excesiva y la inflamación crónica en las enfermedades autoinmunes.
También es un nutriente vital para la función tiroidea adecuada, y los estudios
muestran que el aumento de selenio en
pacientes con tiroides autoinmunes disminuye sus anticuerpos tiroideos.
Zinc. El zinc afecta múltiples aspectos del sistema
inmune, desde la barrera de la piel hasta la regulación génica dentro de los
linfocitos (un tipo de glóbulo blanco). De hecho, el zinc es esencial para la
producción de glóbulos blancos y los estudios muestran que las personas con
deficiencia de zinc son más susceptibles a los patógenos.
Magnesio. El magnesio, que es importante no solo para
la función inmune sino también para la salud del corazón, es un mineral que la
mayoría de la gente tiene bajo en forma crónica debido a los altos niveles de
estrés y las dietas altas en azúcar (el azúcar reduce los niveles de magnesio).
Se ha demostrado que la deficiencia de magnesio causa un aumento en la
producción de citocinas proinflamatorias, lo que aumenta el nivel general de
inflamación y contribuye a la autoinmunidad.
Es indudable la importancia de mantener un
ambiente intestinal en óptimas condiciones de salud, ya que es donde reside
este sistema nervioso entérico y donde se acaban de fabricar todas las
vitaminas, aminoácidos, ácidos grasos esenciales…etc. necesarios para que se
sinteticen las hormonas, neurotransmisores, enzimas…etc. imprescindibles para
una correcta función física y mental.
Más estudios científicos, en el campo de la psiconeuroinmunología, son necesarios
respecto a la inter-relación de estos dos cerebros, al papel que desempeña la
microflora intestinal, la síntesis de neurotransmisores por parte de este
Sistema Nervioso Entérico, y la posibilidad de cruzar la barrera
hematoencefálica atendiendo a determinadas circunstancias físico-químicas de la
misma barrera hematoencefálica o incluso de los neurotransmisores.










